����ŷ���г�һֱ���ڶ౾��ҩ��ҵ��������ѡ�����Բ�Ӱ�춫�˹�����Ϊ�����г��Ĵ���������Ϊȫ������ҽҩ��չDZ�������г�֮һ��
�з�����������ҩ��ʼ���ֶ����г����罨��������ʩ�����������ܲ��Լ��з����ĵȣ��й�������ҵ������ҩҵ�������������ҽҩ�Ͱټ����ݵ�Ҳ��ʼ̽�����˵������»�����
“ҩ�����ƶ���������ʱӦ��������������Ϊ���ĵ�һ·������˼����θ���������ʵ�������в�Ʒ�����ѡ����ȷ����㣬�Ը��͵ķ��վ����ں���ʵ�ֲ�Ʒ���з�����ҵ���ıջ���”����ϣ��ҽѧ�о�����˾��ʼ�˵��������з��ͱ�ʾ��

������ϣ��ҽѧ��ʼ��
�Ⱥ���ְ��Labcorp��Syneos�ȹ�����CRO��˾��ӵ�г���15���ȫ�������ҽҩ�о��������飬�����������̫����ҵ��ŷ��������չҽҩ��Ʒ�з�������
������Ŀǰ�ڹ����ѧ�����ٴ�����ѵ������������������ҵ�ں����г���չҩƷ�з���������Ϊ������ݹ�˾���������Ͳ�Ʒ�ص���ȷ��������Ŀ���г����Զ����г�Ϊ�������������˶��й�ҩ������ļ��⼰���顣
���ѵ�һ·������
�з��ͣ�����ΪΪʲô����������ҩ��˾��������ѡ������
�����
2018��6���й�����ҩƷ�ල��������ѡΪICH��ί���Ա���й�ҩƷע�Ἴ��Ҫ������ʽӹ죬������ҵʹ��ͬһ�����Ͻ�������˫����Ϊ�˿��ܡ�����������ҽҩ��ҵ�Ĵ��¸ߵأ�ͬʱҲ��ȫ���һ��ҽҩ�г���������ҵ��Ϊ����ܽ��������г���ζ�ž�Ĵ��»ر���ͬʱҲ����ҵ���ʻ�ʵ������֤��
����ѡ���ԭ���кܶ࣬�е���ҵ��ʼ�˺�Ͷ����Ϊ�����ֵ�ÿ���ȥ�����걨IND���е���ҵ������Ϊȱ����Ԫ��˼�����жϣ�������Ϊ�����Ŷӻ��ߺ�����CRO��˾����������Դ�ͱ��������߶Ա�Ĺ�˾����������������ȥ��������
�����������Ź��ڴ����ɹ����ߵ�ʵʩ���Լ����ϳ��ֵ��¹�˾ӿ������������������Ϊ�����������˾�ؿ��г����ò�ѡ�IJ��ԡ����ͽ����ϰ��꣬����51����ҵ��������Ȼ�в�����ҵѡ��ŷ�ޡ��ձ������˵ȵأ����������Ǵ������ҵ���ֵ���Ҫ�г�����ʵ�ϣ����ֵ�һ��·��������ɱ�����ҵ�������г�����һ��“�ھ�”����������ҵ�����������Ͳ�Ʒ�����ʺ�������������չ�ٴ��о���
�з��ͣ�������ѡ����ܻ����ҵ�ķ�չ����������Ӱ�죿��ҵ����ΰ���·��������
�����
���ڹ�ȥ��Щ��Ĺ����з��֣���ʵһ���о�����һ���ٴ��������ķ��գ������������δ��ʼ֮ǰ�����ݲ�Ʒ�ص���������ѡ��һ�����ʵĹ��ҡ�������ȷ�ķ���ȥ��չ�ٴ��о������û�н��г�ֵĵ��У���ֱ�ӵ�Ӱ����Ǽ����õ�������������Ʒ���з������Լ��ٴ������ƽ�����ҵ����˳���̶�Ҳ�����ֹۡ�
�Ҿ��ð���FDA��Ҫ���õ��ٴ����������й���˾��˵�Ѿ��кܳ����·�����ص���������õ��ٴ�����֮��Ĺ����Լ����������Ʒ�������г��ľ���DZ���������г���һЩ���ص�Ҫ�������ٴ�����ʵʩ�Լ���Ʒ��ҵ���Ͼ����ܼ��ң��ع˹�ȥ����������������г��ı���ҩ���࣬�����ҵû����������������λ��һ��ʼ�Ͷ��г����ⲻ������йء�
��Ϊ����ƫ�������Ŀ��ꪵ����Ӳ����������������г�����ǰ��Ϊ�й��¹�����������ij����չ�ٴ��о��������й����繫˾Ҳ������������ڵ����ٴ���Դ���������Ŀ�ٴ���Դ���ң�������Ŀ���͡�
����˵���ر������һЩ����Biotech��˾���ڲ��ֺ���ǰ����Ҫ�ۺϿ���һ�³ɱ�������ijɱ��������ʱ��ɱ���Ҳ��������ɱ��Ͳ���ɱ���һ���Ʒ�Ŀ�����Ҫ�������ʽ�ʱ���������Դ��ÿһ�����Ҫ������˵��������Դ����£����ѡ��һ�����ʺϵ����������뵽�Լ��������з����̣��Ƿdz��ؼ��ľ��ߡ�
��ְ��������г��Ļ���
�з��ͣ������˽һЩ������ҵת���˿����г�������Ϊ�����г��������Ļ�����
�����
���ҽ��������߲�������й�ҩ��������������Ĵ��²�Ʒ���������˲����ͺ����쵽“һ��һ·”�ϵĹ��ҡ��¹������£�ȫ��ҽҩ��ҵ�Ĺ�Ӧ����ֳ������ش�ı仯���ܶ���Һ͵����Ĺ�Ӧ��������һЩ���ɵ��͵���ս������˵���ѡ��й�ҽҩ�IJ�����ԱȽϳ�֣���ȫ����߹����У��ر������“һ��һ·”�ϵ�һЩ���˹��ң����¹ڷ��η����������Ҫ��֧�֡�
�й��Ͷ��˸�����ó������Ҳ�������С�ȥ�궫�˺��й���ó����ֵ����������ŷ�ˣ���Ϊ���й�ó���������ľ����塣
����ӵ�н�7���˿ڣ��Դ���ҽҩ��Ʒ�����������Ŀǰ���˳�Ա��ƽ��ҽ��֧��ֻռGDP��4.1%�����ž��õĿ��ٷ�չ����Ԥ��ҽ��֧��ռ�Ȼ�������ǣ���Ӧ�Ķ��˶Դ���ҽҩ��Ʒ�ľ�DZ��������һ���ͷš�
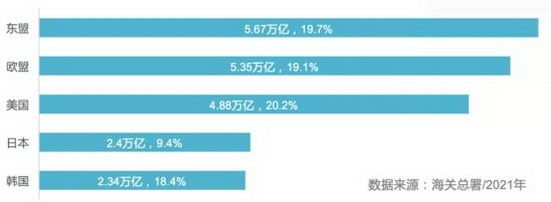
�ڶ��˵������ʼ��Ա���У��¼��µľ��÷�չ�ٶ���죬�˾�GDP������ߣ��ڶ��˵�������һ�ġ��¼�������Ӣ������ң�����ռ�ȳ��߳ɣ�������ͨ�ϰ�С��ҽ��ˮƽλ������ǰ�У��ƴ��������ٴ���������Ҳ�ϸߡ��Աȸ���ÿ�����˿ڵ��ٴ������������¼��½�����������Զ���������������ҡ�
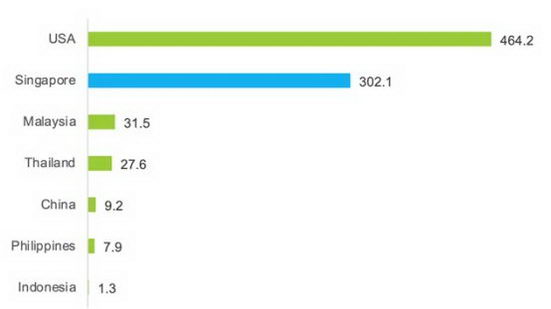
�¼���ÿ�����˿��ٴ�����������ͼƬ��Դ��ϣ��ҽѧ��
�������ı����£���������������ҽҩ�г��Ա���ҩ����˵��ζ�ž�ķ�չ����������ҩ��ѡ�����¼�����Ϊ������֧�㣬���ٽ�������ʻ�������Ȼ����䵽����������������������ŷ������ʧΪһ�ַ��ո��͡�Ч�ʸ��ߵIJ��ԡ�
�з��ͣ�������˾��������������Ҫ����Щ������ΰ��ն����г��IJ��컯���ƣ�
�����
������˾���չ��ʱ��з��IJ�Ʒ�����Կ��ǽ������ˣ����˶�������������ϸ���Ʒ��ȱȽ�ǰ�����Ʒ����Ŀ���Ҳ������̫������⡣
���Ҫѡ������Ϊ�����ĵ�һվ������Ҫ���ǵ��ǵ����Ƿ�߱���ˮƽ�Ŀ�������������ˮƽ�Լ��Ŷ�ȥ����������������˵������з���������λ�Ҫ���Ǹ�������Ծ�����Ӧ֢����Ⱥ����������ˮƽ���г�ǰ����
���������Ҫ��ҽҩ�г������˵������Ƿ�չDZ���Լ۸���Ը����С���ȱ������г��Ƚ���Ƭ����Ҫ�����ϸ���Ա���������չ�о��Ͳ����г���
ͬʱ�����˵ľ���ѹ����Խ�С����Ϊŷ����ҩ�����������һʱ��ѡ���ڶ��˿������µIJ�Ʒ���й���ҵ��ͬ���Ʒ�л����ڸõ�����ʵ���������ۣ���˴�����ҵ�����ʵ�ִ��ٴ���������ҵ�������뵱��ҽ���ɹ�Ŀ¼��������
���Ӧ�Ծ������ս
�з��ͣ��й�ҩ�������չ�ٴ��������ٵ���Ҫ��ս��ʲô�����Ӧ�ԣ�
�����
�ں��չ�ٴ���Ҫ��Գ���Ѱ��������ս�Ժ��ٴ���Ӫ��ս����������Դ��Эͬ���ں�����ٴ������У���κ͵��ص�ҽԺ���ٴ�ר�һ���ʵʩ�Ŷӽ��ܺ������߶�Эͬ��������ҵ��CRO��˾��˵����Ҫ�зḻ�ĺ����ٴ������Ŷ�����ɣ��ⷽ����˲�Ҳһֱ�ȽϽ�ȱ��
Ȼ���������з���ܵĴ����ҵ��Ե��ص������������ɷ��桢ָ��ԭ���רҵϰ���г�ֵ����⣬���ܸ��õ���Ӧ���ص��з�������
��������Ļ���ЭͬҲ�Ǻ�����Ӫ���к���Ҫ��һ����ս�����¼���������������ң����Ƕ��ڿ��������ԵĹ�ͨ������Ҫ�й���ҵ��ȥѧϰ�ͽ����
���������ս��Ҫ��ȷ�Ƽ��ҵ���ȷ���о����������飬�Կ��ٿ����ٴ��о���ͬʱ��Ҫ�ƶ���ȷ�IJ��ԣ����ӿ��о����ȣ�Ŀǰ�����ܹ��ṩ���������CRO���ࡣ���ⷽ�棬ϣ��ҽѧ�����ŶӾ���Ŭ�������һЩ���ۣ�����25��ݵ��о��ߵ�����17��ݵ��о���Ŀ������ͬʱҲ����ȫ��20������ʺ�����鼰ȫ��2000��λ��ҵ��Ӣ������֧�ţ����ǿ��Կ�����ȫ��ҽԺ/�ٴ��о����ģ�ȷΪ��Ŀ�ƶ����ԣ�ƥ�䵽����ʵ��о��ߡ�
�з��ͣ�̸�����������ɱ����Ҫ���ǵ����ݻ��ϵ����⡣������Ҫҽҩ�г������ݻ����Ƿ�ṹ����ս����ҵ�����Ӧ�ԣ�
�����
���ݻ�����ʵ�Ǹ�α���⡣�����������dz����й����ݵģ��������й����ݲ�����ֻ���й����ݾͿ��ԣ����Ϻ��������Ҳ������ֻ�ú������ݾͿ��Ի����������3������FDA�ܾ����й�ij��ҵ������Ʒ���������룬FDA�ᵽ��ǰ���������̫��һ��û�г��������Ⱥ�ֲ�����������Ҫ���չ��������ٴ��о���
��ʵ�ϣ������ܷ��ϵı����ǿ�ѧ���⣬�������������⡣�ڼ�����ʵ��������Ҳ���������������Է������ǵ�һ��Сɽ�壬ֻҪ�ϸ��չ淶��չ�ٴ��о�������ͬ�����Ի���Ͽɡ�����ҩ�ಿ���ܷ������Ӧ��������Ʒ���У���Ҫ����Щ�����ܷ��ֻش�ҩ�ಿ�Ź�ע�Ŀ�ѧ���⡣
������ҵ��˵�����۳����ĵ�һվѡ����������ն�ϣ���ܹ�����������ŷ�ޡ��ձ���Щ��Ҫ���г�������һ��ʼ�Ͳ��ܴ��ڽ���������Ӧ���Թ��������ϸ�ı���Ҫ������չ�ٴ��о����Ա��ں����Ŀ�����֧�ֲ�Ʒ���������г���